Тема Количественный анализ
- На титрование 15мл раствора гидроксида натрия затрачено 20мл 0,09М раствора соляной кислоты. Масса щелочи в 500мл этого раствора равна … г
- При добавлении избытка разбавленного раствора карбоната аммония к 50 мл 0,2М раствора
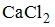 образуется осадок массой _____ г
образуется осадок массой _____ г - В основе титриметрического анализа лежит закон…
- Объем 0,5М раствора соляной кислоты, необходимый для полной нейтрализации 50 мл 0,2М раствора Ba(OH)2
- Задание оценивается в 3 балла
Сточные воды металлургического производства содержат растворимые соединения серебра, стронция, железа(III), хрома(III) и меди (II). Используя систематический анализ кислотно-щелочным методом, расположите реагенты, последовательным действием которых, можно разделить данные катионы - Чтобы получить 0,1н раствор соляной кислоты HCl, к 200 мл 0,125н раствора следует добавить ____ мл воды
- Задание оценивается в 5 баллов
На титрование сильно минерализованной воды в аммиачном буфере в присутствии эриохромового черного было израсходовано 13,6 мл 0,0250 М раствора ЭДТА. На титрование такого же объема воды в присутствии избытка гидроксида натрия и индикатора кальцеина затрачено 9,6 мл
0,0250 М раствора ЭДТА. Суммарное содержание ионов кальция и магния в минеральной воде составляет _____ мг/л (с точностью до целых,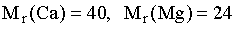 )
) - На титрование 25 мл раствора гидроксида калия затрачено 20 мл раствора азотной кислоты с молярной концентрацией 0,1моль/л. Масса щелочи в 500 мл этого раствора равна ___ грамма
- На титрование 20мл раствора NaOH израсходовано 25мл 0,08М HCl. Масса щелочи в 200мл этого раствора равна … г
- Задание оценивается в 5 баллов
Из пробы сточной воды промышленного предприятия объемом 100 мл осадили сульфат-ионы раствором хлорида бария. Осадок выделили и растворили в 25,0 мл 0,0250 М раствора ЭДТА. На титрование избытка ЭДТА в аммиачном буфере в присутствии эриохромового черного раствором сульфата магния было израсходовано 9,0 мл 0.0250 М раствора MgSO4. Содержание сульфат-ионов в пробе воды составляет _____ мг/л (с точностью до целых,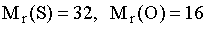 )
) - При определении концентрации соляной кислоты в растворе методом кислотно-основного титрования в качестве индикатора используется …
- Задание оценивается в 3 балла
Сточные воды металлургического производства содержат растворимые соединения магния, бария, цинка, серебра и меди (II). Используя систематический анализ кислотно-щелочным методом, расположите реагенты, последовательным действием которых, можно разделить данные катионы - Задание оценивается в 5 баллов
На титрование сильно минерализованной воды в аммиачном буфере в присутствии эриохромового черного было израсходовано 13,6 мл 0,0250 М раствора ЭДТА. На титрование такого же объема воды в присутствии избытка гидроксида натрия и индикатора кальцеина затрачено 9,6 мл
0,0250 М раствора ЭДТА. Суммарное содержание ионов кальция и магния в минеральной воде составляет _____ мг/л (с точностью до целых,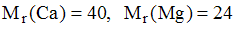 )
) - На титрование 15 мл раствора гидроксида натрия затрачено 20 мл 0,09М раствора соляной кислоты. Масса щелочи в 500 мл этого раствора равна ___ грамма
- Для установления титра раствора перманганата калия применяется стандартный раствор …
- Объем 0,1 М раствора хлорида бария, необходимый для осаждения сульфат-ионов из 200 мл 0,025 М раствора серной кислоты, равен ____ мл
- Для осаждения хлорид-ионов из 200мл 0,1М раствора соляной кислоты требуется раствор, содержащий ___ граммов нитрата серебра
- Задание оценивается в 3 балла
Сточные воды металлургического производства содержат растворимые соединения магния, кальция, цинка, свинца и никеля (II). Используя систематический анализ кислотно-щелочным методом, расположите реагенты, последовательным действием которых, можно разделить данные катионы - Объем 0,1 М раствора
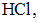 необходимый для нейтрализации раствора гидроксида натрия, содержащего 0,08 г
необходимый для нейтрализации раствора гидроксида натрия, содержащего 0,08 г 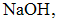 равен ____ мл
равен ____ мл - Количество моль NaOH, необходимое для нейтрализации 3,65 г HCl
- При титровании 20 мл раствора азотной кислоты затрачено 15 мл 0,12М раствора NaOH. Масса кислоты в 250 мл этого раствора равна ___ грамма
- Для нейтрализации 50 мл раствора гидроксида бария c молярной концентрацией 0,2 моль/л потребуется _____ мл раствора соляной кислоты c молярной концентрацией 0,1 моль/л
- Объем 0,1 М раствора
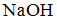 , необходимый для нейтрализации раствора серной кислоты, содержащего 0,147 г
, необходимый для нейтрализации раствора серной кислоты, содержащего 0,147 г 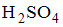 , равен ____ мл
, равен ____ мл - Задание оценивается в 3 балла
Для определения содержания ионов железа в сточной воде промышленного предприятия пробу объемом 250 мл обработали окислителем и осадили железо действием аммиака. Выделенный осадок растворили в соляной кислоте и оттитровали раствором ЭДТА в присутствии сульфосалициловой кислоты. На титрование было израсходовано 10,9 мл 0.0250 М раствора ЭДТА. Содержание ионов железа в сточной воде составляет ______ мг/л
(с точностью до целых,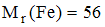 )
) - При гравиметрическом определении свинца в сплаве получено 1,4642 г PbSO4. Масса свинца в сплаве составляет _______ грамм(–а)
- Для нейтрализации 100 мл 0,2М раствора азотной кислоты необходим раствор, содержащий _____ граммов гидроксида натрия
- Задание оценивается в 5 баллов
Галогенид щелочного металла массой 0,2374 г растворили в воде и объем раствора довели до 100 мл. Полученный раствор оттитровали раствором нитрата серебра в присутствии хромата натрия в качестве индикатора. На титрование было израсходовано 19,0 мл 0,1050 М раствора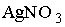 . Название исходного галогенида (введите полное название) …
. Название исходного галогенида (введите полное название) … - Задание оценивается в 5 баллов
Cульфат двухвалентного металла массой 0,1689 г растворили в 25,0 мл
0,050 М раствора ЭДТА. На титрование избытка ЭДТА в аммиачном буфере в присутствии эриохромового черного раствором сульфата магния было израсходовано 10,5 мл 0.050 М раствора MgSO4. Название исходного вещества (введите полное название) … - Индикатором, который применяется при комплексонометрическом определении жесткости воды трилоном Б, является …
- При титровании раствора, содержащего 0,1 г вещества, израсходовано 21,5 мл 0,1М раствора HCI. Массовая доля гидроксида натрия в образце равна …
- Объем 0,1 М раствора
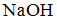 , необходимый для осаждения железа в виде гидроксида из 20 мл 0,05 М раствора нитрата железа (III), равен ____ мл
, необходимый для осаждения железа в виде гидроксида из 20 мл 0,05 М раствора нитрата железа (III), равен ____ мл - Объем 0,15н раствора серной кислоты, необходимый для осаждения ионов бария из 60 мл 0,2н раствора хлорида бария, равен …
- Задание оценивается в 5 баллов
На титрование пробы минеральной воды объемом 100 мл в аммиачном буфере в присутствии эриохромового черного было израсходовано 16,8 мл 0,0250 М раствора ЭДТА. После отделения кальция в виде оксалата на титрование оставшегося раствора в тех же условиях затрачено 7,4 мл раствора ЭДТА той же концентрации. Содержание ионов кальция в минеральной воде составляет _____ мг/л (с точностью до целых,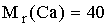 )
) - Объем 0,5М раствора соляной кислоты, необходимый для полной нейтрализации 50 мл 0,2н раствора Ba(OH)2
- При титровании 15мл раствора азотной кислоты израсходовано 20мл 0,03М раствора гидроксида калия. Масса кислоты в 500мл этого раствора равна … г
- Объем 0,5М раствора соляной кислоты, необходимый для нейтрализации 50 мл 0,2М раствора гидроксида натрия, равен ___ миллилитрам
- Задание оценивается в 3 балла
Сточные воды металлургического производства содержат растворимые соединения марганца (II), бария, кадмия, серебра и хрома(III). Используя систематический анализ кислотно-щелочным методом, расположите реагенты, последовательным действием которых, можно разделить данные катионы - Количество азотной кислоты, содержащейся в растворе, на нейтрализацию которого израсходовано 100мл 0,2М раствора NaOH, составляет ___ моль
- Объем 0,1н раствора КОН, необходимый для нейтрализации 20 мл 0,15н раствора азотной кислоты, равен …
- При определении содержания бромида калия в сточных водах на титрование аликвоты объемом 100 см3 было израсходовано 12,0 мл раствора нитрата серебра с молярной концентрацией 0,0125 моль/л. Содержание бромида калия в водах составляет _____ мг/л
- На титрование 25мл раствора соляной кислоты затрачено 20мл 0,15М раствора гидроксида калия. Масса хлороводорода в 500мл этого раствора равна … г
- Количество моль NaOH, необходимое для нейтрализации 3,65 г HCl
- При сливании 20 мл 0,1М раствора
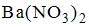 и 15 мл 0,2М раствора
и 15 мл 0,2М раствора 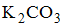 образуется осадок массой _____ г
образуется осадок массой _____ г - Задание оценивается в 5 баллов
На титрование пробы минеральной воды объемом 100 мл в аммиачном буфере в присутствии эриохромового черного было израсходовано 16,8 мл 0,0250 М раствора ЭДТА. После отделения кальция в виде оксалата на титрование оставшегося раствора в тех же условиях затрачено 7,4 мл раствора ЭДТА той же концентрации. Содержание ионов кальция в минеральной воде составляет _____ мг/л (с точностью до целых,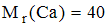 )
) - Объем 0,15н раствора серной кислоты, необходимый для осаждения ионов бария из 60 мл 0,2н раствора хлорида бария, равен ___ миллилитрам
- на титрование раствора, содержащего 0,0375 г нитрита натрия NaNO2 израсходовано 20 мл 0,05н раствора KMnO4. Массовая доля чистого NaNO2 в образце
- Количество азотной кислоты, содержащейся в растворе, на нейтрализацию которого израсходовано 100мл 0,2М раствора NaOH, составляет ___ моль
- Объем раствора хлорида кальция c молярной концентрацией 0,1 моль/л, необходимый для осаждения карбонат-ионов из 200мл раствора карбоната калия c молярной концентрацией 0,15 моль/л, равен ___ миллилитрам
- Масса осадка, образующегося при сливании 200мл 0,1М раствора карбоната натрия и 100мл 0,15М раствора хлорида кальция, равна ____ граммов
- При определении бария весовым методом из 2,0000 г анализируемого образца получено 0,1165 г сульфата бария. Массовая доля бария в образце равна ___ %
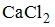 образуется осадок массой _____ г
образуется осадок массой _____ г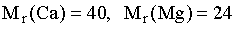 )
)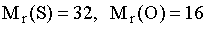 )
)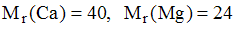 )
)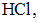 необходимый для нейтрализации раствора гидроксида натрия, содержащего 0,08 г
необходимый для нейтрализации раствора гидроксида натрия, содержащего 0,08 г 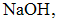 равен ____ мл
равен ____ мл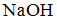 , необходимый для нейтрализации раствора серной кислоты, содержащего 0,147 г
, необходимый для нейтрализации раствора серной кислоты, содержащего 0,147 г 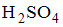 , равен ____ мл
, равен ____ мл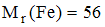 )
)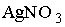 . Название исходного галогенида (введите полное название) …
. Название исходного галогенида (введите полное название) …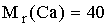 )
)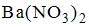 и 15 мл 0,2М раствора
и 15 мл 0,2М раствора 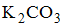 образуется осадок массой _____ г
образуется осадок массой _____ г )
)