Тема Химическая кинетика
- Задание оценивается в 3 балла
Начальные концентрации оксида азота (II) и кислорода в системе
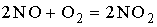 составляли 0,5моль /л и 0,4 моль/л соответственно. К моменту, когда прореагирует 80% исходного количества оксида азота (II), скорость реакции уменьшится в ____ раз
составляли 0,5моль /л и 0,4 моль/л соответственно. К моменту, когда прореагирует 80% исходного количества оксида азота (II), скорость реакции уменьшится в ____ раз - Задание оценивается в 3 балла
Начальные концентрации оксида азота (II) и кислорода в системе
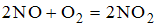 составляли 0,5моль /л и 0,4 моль/л соответственно. К моменту, когда прореагирует 80% исходного количества оксида азота (II), скорость реакции уменьшится в ____ раз
составляли 0,5моль /л и 0,4 моль/л соответственно. К моменту, когда прореагирует 80% исходного количества оксида азота (II), скорость реакции уменьшится в ____ раз - Задание оценивается в 3 балла.
Значение энергии активации химической реакции, для которой температурный коэффициент в интервале температур 200 - 300С равен 3 составляет (с точностью до целых) ____ кДж/моль - Задание оценивается в 3 балла
В сосуд объемом 10 л при температуре 700 К поместили 13г водорода и 508г паров йода. К моменту образования в системе 384 г йодоводорода скорость прямой реакции уменьшится в ____ раза - Задание оценивается в 5 балла
Реакция С6Н5N2Cl → С6Н5Cl + N2 является реакцией первого порядка. Константы скорости этой реакции при температурах 323К и 373К равны соответственно 1,8∙102с-1 и 6,8∙102 с-1. Время, в течение которого реакция пройдет на 90% при температуре 353К составляет_____ cекунды - Задание оценивается в 3 балла
Минимальное и максимальное значения энергии активации для химической реакции, к которой применимо правило Вант-Гоффа в интервале температур 200 – 300С, равны соответственно (с точностью до целых) ____ и ____ кДж/моль - Задание оценивается в 3 балла.
Минимальное и максимальное значения энергии активации для химической реакции, к которой применимо правило Вант-Гоффа при 250 С, равны соответственно (с точностью до целых) ____ и ____ кДж/моль - Задание оценивается в 5 балла
Константы скорости реакции первого порядка при температурах 343 и 403 К равны соответственно 3,4∙10-3 и 1,1 с-1.Скорость этой реакции при температуре 363К в начальный момент времени при концентрации исходного вещества 0,01 моль/л составляет ____ моль/(л∙с) - Задание оценивается в 3 балла
Реакция протекает в газовой фазе по схеме 2А + В → С.
Константа скорости реакции при температуре реакции равна 0,4 л2∙с2 /моль2.
Начальные концентрации реагентов А и В составляли соответственно 0, 7 моль/л и 0,4моль/л. После того, как прореагирует 25% вещества В, скорость реакции при той же температуре составит _____ моль/л∙с - Задание оценивается в 3 балла
В сосуд объемом 10 л ввели 6,4 г оксида серы (IV) и 7,68 г кислорода. К моменту, когда прореагирует 80% оксида серы (IV), скорость реакции (считать ее элементарной) уменьшится в _____ раз - Задание оценивается в 3 балла
В сосуд объемом 10л ввели 45г оксида азота (II) и 71 г хлора. К моменту, когда прореагирует 60% хлора, скорость реакции уменьшится в ____ раза - Задание оценивается в 5 балла
Реакция термического разложения этана С2Н6 → С2Н4 +О2 является реакцией первого порядка. Константы скорости этой реакции при температурах 823К и 863К равны соответственно 2,5∙105с-1 и 2,1106 с-1 .При температуре 893К константа скорости реакции составит _____ с-1 - Задание оценивается в 5 балла
Константы скорости реакции второго порядка при температурах 298 и 348К равны соответственно 1,8∙10-4 и 2,7∙10-2 л∙с/моль. Скорость этой реакции при температуре 328К в начальный момент времени при концентрациях обоих исходных веществ 0,1 моль/л составляет _____ моль/(л∙с) - Задание оценивается в 3 балла
В сосуд объемом 10 л ввели 6,4 г оксида серы (IV) и 7,68 г кислорода. К моменту, когда прореагирует 80% оксида серы (IV), скорость реакции уменьшится в _____ раз - Задание оценивается в 5 балла
Реакция разложения оксида азота N2O5 → N2O4 +1/2О2 является реакцией первого порядка. Константы скорости этой реакции при температурах 273К и 333К равны соответственно 0,41∙10-6с-1 и 0,9∙10-3 с-1. Время, в течение которого реакция пройдет на 60% при температуре 313К, составляет __ часа
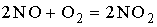 составляли 0,5моль /л и 0,4 моль/л соответственно. К моменту, когда прореагирует 80% исходного количества оксида азота (II), скорость реакции уменьшится в ____ раз
составляли 0,5моль /л и 0,4 моль/л соответственно. К моменту, когда прореагирует 80% исходного количества оксида азота (II), скорость реакции уменьшится в ____ раз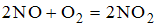 составляли 0,5моль /л и 0,4 моль/л соответственно. К моменту, когда прореагирует 80% исходного количества оксида азота (II), скорость реакции уменьшится в ____ раз
составляли 0,5моль /л и 0,4 моль/л соответственно. К моменту, когда прореагирует 80% исходного количества оксида азота (II), скорость реакции уменьшится в ____ раз