Тема Количественный анализ
- После соответствующей обработки навески 4,6080 г каменного угля и осаждения получили 0,4194 г сульфата бария. Массовая доля (%) серы в угле
- Задание оценивается в 5 баллов
Из пробы сточной воды промышленного предприятия объемом 100 мл осадили сульфат-ионы раствором хлорида бария. Осадок выделили и растворили в 25,0 мл 0,0250 М раствора ЭДТА. На титрование избытка ЭДТА в аммиачном буфере в присутствии эриохромового черного раствором сульфата магния было израсходовано 9,0 мл 0.0250 М раствора MgSO4. Содержание сульфат-ионов в пробе воды составляет _____ мг/л (с точностью до целых,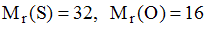 )
) - Объем 0,2н раствора H2SO4, необходимый для осаждения ионов бария из 100 мл 0,2н раствора BaCl2
- Масса осадка, образующегося при сливании 50 мл 0,2М раствора нитрата серебра и 100 мл 0,1М раствора хлорида натрия, равна …
- На титрование 20,00 см3 0,10 М раствора HCl требуется 16,00 см3 раствора КОН. Следовательно, молярная концентрация щелочи составляет ___________ моль/дм3
- Для установления точной концентрации кислот в качестве первичных стандартных веществ используются …
- В основе методов кислотно-основного титрования лежит процесс образования …
- Для нейтрализации 40мл 0,5М раствора уксусной кислоты требуется раствор содержащий ____ моль гидроксида натрия
- Методы анализа, основанные на измерении объема раствора реагента с точно известной концентрацией, затраченного на взаимодействие с определенным объемом раствора определяемого вещества, называются …
- Масса осадка, образующегося при сливании 50 мл 0,2М раствора нитрата серебра и 100 мл 0,1М раствора хлорида натрия, равна ___ грамма
- Задание оценивается в 3 балла
Для определения содержания хлорид-ионов в минеральной воде пробу объемом 100 мл оттитровали раствором нитрата серебра в присутствии хромата натрия в качестве индикатора. На титрование было израсходовано 12,4 мл 0,0250 М раствора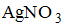 . Содержание хлорид-ионов в минеральной воде составляет _____ мг/л (с точностью до целых,
. Содержание хлорид-ионов в минеральной воде составляет _____ мг/л (с точностью до целых, 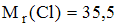 )
) - Задание оценивается в 3 балла
Для определения содержания хлорид-ионов в минеральной воде пробу объемом 100 мл оттитровали раствором нитрата серебра в присутствии хромата натрия в качестве индикатора. На титрование было израсходовано 12,4 мл 0,0250 М раствора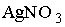 . Содержание хлорид-ионов в минеральной воде составляет _____ мг/л (с точностью до целых,
. Содержание хлорид-ионов в минеральной воде составляет _____ мг/л (с точностью до целых, 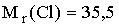 )
) - Задание оценивается в 3 балла
Для определения содержания ионов кальция в воде минерального источника пробу объемом 100 мл оттитровали раствором ЭДТА в присутствии избытка гидроксида натрия и индикатора кальцеина. На титрование было израсходовано 13,5 мл 0.010 М раствора ЭДТА. Содержание ионов кальция в воде составляет _____ мг/л (с точностью до целых,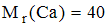 )
) - На полную нейтрализацию раствора серной кислоты затрачено 20 мл 0,1М раствора NaOH. Масса серной кислоты в оттитрованном растворе
- Объем 0,1М раствора карбоната натрия, необходимый для осаждения ионов кальция из раствора, содержащего 0,324 г его гидрокарбоната, равен _____ мл
- Для осаждения хлорид-ионов из 200мл 0,1М раствора соляной кислоты требуется раствор, содержащий ___ грамма нитрата серебра
- При титровании 20мл раствора уксусной кислоты затрачено 16мл 0,15М раствора КОН. Масса CH3COOH в 200мл этого раствора равна … г
- Количество азотной кислоты, содержащееся в растворе, на нейтрализацию которого израсходовано 100мл раствора NaOH c молярной концентрацией 0,2 моль/л, составляет ___ моль
- Для нейтрализации 100 мл раствора гидроксида натрия c молярной концентрацией 0,2 моль/л потребуется _____ мл раствора серной кислоты c молярной концентрацией 0,1 моль/л
- На титрование 25 мл раствора гидроксида калия затрачено 20 мл 0,1М раствора азотной кислоты. Масса щелочи в 500 мл этого раствора равна ___ грамма
- При анализе сплава из навески 1,3162 г получено 0,1234 г Al2O3. Массовая доля алюминия в сплаве
- На полную нейтрализацию раствора серной кислоты затрачено 20 мл 0,1М раствора NaOH. Масса серной кислоты в оттитрованном растворе
- Для нейтрализации 100 мл 0,2М раствора азотной кислоты необходим раствор, содержащий _____ грамма(ов) гидроксида натрия
- Объем 0,1М раствора NaOH, необходимый для нейтрализации 20 мл 0,1М HCl…
- Навеску 0,1120 г гидроксида калия КОН растворили в мерной колбе на 100 мл. Молярная концентрация (моль/л) КОН
- Объем 0,2н раствора серной кислоты, необходимый для нейтрализации 40 мл 0,15н раствора гидроксида натрия, равен ___ миллилитрам
- На титрование 25 мл раствора соляной кислоты затрачено 20 мл 0,15М раствора гидроксида калия. Масса хлороводорода в 500 мл этого раствора равна ___ грамма
- При определении железа весовым методом из 1 г анализируемого образца получено 0,32 г оксида железа (III). Массовая доля железа в образце равна ___ %
- Задание оценивается в 3 балла
Сточные воды металлургического производства содержат растворимые соединения стронция, свинца, цинка, никеля (II) и железа (III). Используя систематический анализ кислотно-щелочным методом, расположите реагенты, последовательным действием которых, можно разделить данные катионы - При титровании 15 мл раствора азотной кислоты израсходовано 20 мл 0,03М раствора гидроксида калия. Масса кислоты в 500 мл этого раствора равна ___ грамма
- При титровании раствора, содержащего 0,015 г образца удобрения израсходовано 10,5 мл раствора нитрата серебра с молярной концентрацией 0,015 моль/л. Массовая доля хлорида калия в образце равна ___ %
- Массовая доля серы в угле, из 5,0000 г которого после проведения необходимых аналитических операций было получено 0,4660 г сульфата бария, составляет _____ %
- Масса осадка, образующегося при смешивании 100мл 0,1М раствора FeCl3 и 150мл 0,2М раствора NaOH, равна ___ грамма
- Задание оценивается в 3 балла
Для определения содержания гидрокарбонат-ионов в минеральной воде пробу объемом 100 мл оттитровали раствором соляной кислоты в присутствии метилового оранжевого. На титрование было израсходовано 11,8 мл 0,0150 М раствора HCl. Содержание гидрокарбонат-ионов в минеральной воде составляет _____ мг/л (с точностью до целых) - Титрование по реакции
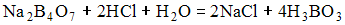 относится к методу ___________ титрования
относится к методу ___________ титрования - Задание оценивается в 3 балла
Для определения содержания ионов железа в сточной воде промышленного предприятия пробу объемом 250 мл обработали окислителем и осадили железо действием аммиака. Выделенный осадок растворили в соляной кислоте и оттитровали раствором ЭДТА в присутствии сульфосалициловой кислоты. На титрование было израсходовано 10,9 мл 0.0250 М раствора ЭДТА. Содержание ионов железа в сточной воде составляет ______ мг/л
(с точностью до целых,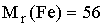 )
) - На титрование 25 мл раствора NaOH израсходовали 22,5 мл 0,1н раствора HCl. Титр NaOH ________ г/мл
- При определении концентрации щелочи в растворе методом кислотно-основного титрования в качестве индикатора используется …
- При титровании 15мл раствора хлорной кислоты (HClO4) потребовалось 20мл 0,1М раствора NaOH. Масса кислоты в 500мл этого раствора равна…
- При анализе сплава на содержание серебра из навески 0,1058 г получено 0,1196 г хлорида серебра AgCl. Массовая доля (%) серебра в сплаве
- Объем 0,1н раствора КОН, необходимый для нейтрализации 20 мл 0,15н раствора азотной кислоты, равен ___ миллилитрам
- Задание оценивается в 5 баллов
Галогенид щелочного металла массой 0,2374 г растворили в воде и объем раствора довели до 100 мл. Полученный раствор оттитровали раствором нитрата серебра в присутствии хромата натрия в качестве индикатора. На титрование было израсходовано 19,0 мл 0,1050 М раствора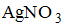 . Название исходного галогенида (введите полное название) …
. Название исходного галогенида (введите полное название) … - При определении содержания сульфата калия гравиметрическим методом, из 2г анализируемого образца содержащего сульфат калия, получено 2,33г BaSO4. Массовая доля K2SO4 в образце равна … %
- При гравиметрическом определении кальция в виде CaC2O4 весовой формой является…
- При титровании 15 мл КОН израсходовано 12 мл 0,1М раствора HNO3. Масса щелочи в 200 мл этого раствора равна ___ грамма
- Для осаждения хлорид-ионов из 200мл раствора соляной кислоты c молярной концентрацией 0,1 моль/л требуется раствор, содержащий ___ грамма нитрата серебра
- При титровании 15 мл раствора хлорной кислоты (HClO4) потребовалось 20 мл раствора NaOH с молярной концентрацией 0,1моль/л. Масса кислоты в 500 мл этого раствора равна ___ грамма
- При титровании 15мл КОН израсходовано 12мл 0,1М раствора HNO3. Масса щелочи в 200мл этого раствора равна … г
- Объем 0,1М раствора хлорида кальция, необходимый для осаждения карбонат-ионов из 200мл 0,15м раствора карбоната калия, равен ___ миллилитрам
- Задание оценивается в 3 балла
Для определения содержания хлорида натрия в галите пробу раствора, содержащего 0,0947 г минерала, объемом 100 мл оттитровали раствором нитрата серебра в присутствии хромата натрия в качестве индикатора. На титрование было израсходовано 14,8 мл 0,1050 М раствора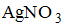 . Массовая доля хлорида натрия в галите составляет _____ % (с точностью до целых,
. Массовая доля хлорида натрия в галите составляет _____ % (с точностью до целых, 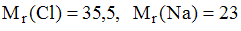 )
)
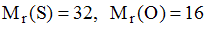 )
)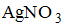 . Содержание хлорид-ионов в минеральной воде составляет _____ мг/л (с точностью до целых,
. Содержание хлорид-ионов в минеральной воде составляет _____ мг/л (с точностью до целых, 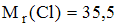 )
)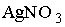 . Содержание хлорид-ионов в минеральной воде составляет _____ мг/л (с точностью до целых,
. Содержание хлорид-ионов в минеральной воде составляет _____ мг/л (с точностью до целых, 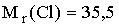 )
)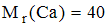 )
)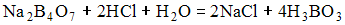 относится к методу ___________ титрования
относится к методу ___________ титрования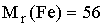 )
)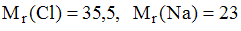 )
)